کارسینوم هپاتوسلولار (HCC-Hepatocellular Carcinoma) یکی از شایعترین سرطانها و یکی از علل اصلی مرگ و میر در سراسر جهان است. بیش از 75 درصد بیماران HCC از نظر علت با عفونت مزمن هپاتیت Hepatitis B Virus -HBV) B) در منطقه آسیا و اقیانوسیه مرتبط هستند. غربالگری افراد در معرض خطر، از جمله مبتلایان به سیروز و هپاتیت ویروسی، راهی برای بهبود بقا فراهم میکند، اما روشهای غربالگری فعلی ناکافی هستند. سرطان کبد چهارمین علت عمده مرگ و میر ناشی از سرطان در جهان محسوب میشود و به دلیل افزایش آمار مبتلایان به چاقی و دیابت نوع دو، به سرعت در حال گسترش است. این بیماری معمولاً در افراد بالای ۵۰ سال و به خصوص در مردان دیده میشود. سیروز یا زخمشدن کبد، هپاتیت B وC ، عفونت ویروسی، التهاب مزمن کبد، هموکروماتوز (تجمع آهن در بدن) و مصرف الکل، مهمترین دلایل ابتلا به سرطان کبد هستند.
کبد با 36/1 کیلوگرم وزن، بزرگترین عضو داخلی بدن است که بیش از ۵۰۰ عملکرد حیاتی را کنترل میکند. مهمترین وظیفه کبد، فیلترکردن خونی است که از دستگاه گوارش وارد کبد میشود و قرار است در سراسر بدن جریان یابد. تمام مواد سمی و مضر خون در کبد جدا میشوند. کبد با تولید صفرا، چربی غذا را تجزیه کرده و آن را تبدیل به انرژی میکند. ذخیره قند بدن نیز به عهده کبد است. تولید و سنتز عناصر مهم پلاسمای خون و ذخیره برخی از مواد مغذی از جمله ویتامینها و آهن نیز بر عهده کبد است. سم زدایی، تنظیم هورمون، سنتز پروتئین، هضم غذا و تجزیه سلولهای قرمز خون نیز از مهمترین وظایف کبد به شمار میآیند. مراحل اولیه بیماریهای کبد هیچ علایمی ندارد. بنابراین کوچکترین نشانهای نیز باید جدی گرفته شود. زرد شدن پوست و چشم، شکم درد مزمن، تورم شکم، خارش مداوم پوست، ادرار تیره، مدفوع کم رنگ یا خونی، خستگی، تهوع، کبود شدن پوست و از دست دادن اشتها، مهمترین علایم بیماریهای کبد هستند.
روشهای مرسوم تشخیص
روشهای درمانی، از جمله جراحی و فرسایش با فرکانس رادیویی، اصلیترین راههای درمانی برای بیماران HCC در مراحل اولیه است. بنابراین، شناسایی بیومارکرهای پیش آگهی برای هدایت تصمیمات درمانی، به ویژه در بیمارانی که درمانهای رادیکال دارند، از اهمیت اولیه برخوردار است. در حال حاضر، برخی از نشانگرهای زیستی جدید، مانند miR-181a-5p7 و VEGFA،به عنوان شاخصهای پیش آگهی بالقوه بیماران HCC گزارش شدهاند. با این حال، این نشانگرهای زیستی هنوز برای کاربردهای بالینی نیاز به اعتبار بیشتر دارند. تا به امروز، تنها نشانگر زیستی مبتنی بر خون در دسترس بالینی برای نظارت بر HCC، آلفا فتوپروتئین (Alpha-Fetoprotein-AFP) است، در حالی که کاربرد بالینی آن به دلیل حساسیت و اختصاصیت کم به شدت محدود شده است.
آزمایش AFP خون
این آزمایش به طور خاص برای اندازه گیری میزان پروتئین آلفا-فتوپروتئین در سرم (AFP) انجام میشود. متاسفانه فقط در حدود نیمی از تومورها میزان بالایی از AFP را میخوانند. بنابراین معمولاً یک تست AFP عادی خون وجود سرطان کبد را نشان نمیدهد. به همین دلیل، مسئله با در نظر گرفتن این واقعیت که AFP با تکثیر سلولهای کبدی نیز تولید میشود، پیچیدهتر میشود. بنابراین کسی که مبتلا به سیروز و بازسازی کبد است احتمالاً سطح AFP را از قبل افزایش داده است. در نتیجه پزشکان اکثراً مایل هستند که بررسی کنند آیا سطح AFP خون ثابت است یا خیر. افزایش سطح AFP بیشتر نشان دهنده HCC است. حتی در مواردی که هیچ علامت قابل تشخیصی در افراد مبتلا به سیروز نبوده و AFP غیرطبیعی ندارند ، باز هم خطر ابتلا به سرطان کبد زیاد است. هر کسی که مبتلا به سیروز و AFP بالا باشد، به ویژه با افزایش پیوسته سطح AFP، به احتمال زیاد یا دچار سرطان کبد میشود یا قبلاً دچار آن شده است.
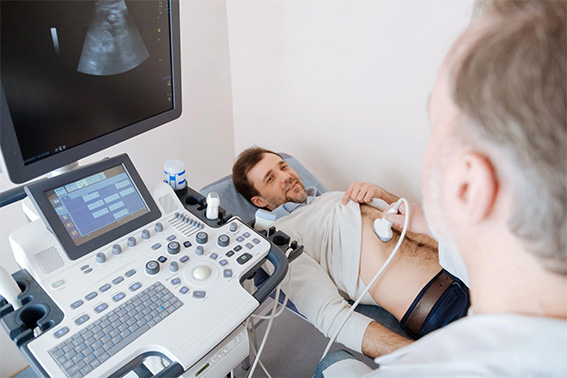
سونوگرافی از کبد
سونوگرافی معمولاً اولین آزمایش غربالگری است که در صورت مشکوک بودن به سرطان کبد HCC انجام میشود. دقت سونوگرافی بستگی زیادی به تکنسین یا رادیولوژیستی دارد که اسکن را انجام میدهد. برخی از اپراتورهای باتجربه ممکن است بتوانند ضایعات (نواحی از بافت غیرطبیعی) را به اندازه ۰٫۵ سانتی متر تشخیص دهند. سونوگرافی دارای مزایایی مانند عدم اشعه یونیزان و ماده حاجب داخل وریدی (تزریق ماده شیمیایی به بدن برای بهبود کنتراست تصویربرداری) است. هزینه سونوگرافی نیز از سایر اسکنها کمتر است.
سی تی اسکن از کبد
هنگامی که با استفاده از ماده بهبود دهنده کنتراست تصویربرداری انجام میشود، سی تی اسکن میتواند به اندازه سونوگرافی حساس باشد، چرا که عامل تصویربرداری از سیستم شریانی و وریدی را بهبود میبخشد. سی تی اسکن نسبت به سونوگرافی به میزان کمتری به اپراتور وابسته است. همچنین این مزیت را دارد که میتواند از مناطق بیشتری از بدن تصویر تهیه کند. سی تی اسکن به طور قابل توجهی گرانتر از سونوگرافی است و افراد را در معرض اشعه یونیزان قرار میدهد.
آنژیوگرافی کبدی
در این روش کاتتری به شریان کبدی وارد میشود و مادهای داخل وریدی به کبد تزریق میشود. این کار ممکن است برای ارزیابی ضایعات دشوار مفید باشد اما شامل خطرات تابش یونیزان، سوراخ شدن شریانی و قرار گرفتن ماده حاجب است. آنژیوگرافی کبدی معمولاً در افرادی انجام میشود که در معرض خطر بالایی هستند اما با سایر آزمایشها و تصویربرداریها نتوانستهاند نشانهای از سرطان کبد HCC بیابند. در زمان آنژیوگرافی و در صورت تشخیص تومور، ممکن است تصمیم گرفته شود که شریان تغذیه کننده تومور پیش از تزریق داروهای ضد سرطان به آن مسدود شود (شیمی آمبولی).
تصویربرداری تشدید مغناطیسی (MRI) از کبد
استفاده از روش (Magnetic Resonance Imaging (MRI برای تشخیص تومورهای کبدی بسیار محبوب است. این روش مانند سی تی اسکن میتواند نواحی زیادی از قفسه سینه و شکم را در یک جلسه بررسی کند. اما از آنجا که هیچ اشعه یونیزانی درگیر نیست، تصویربرداری میتواند بارها و با خطر کم تکرار شود. این فناوری تا آنجا پیشرفت کرده است که MRI های جدیدتر میتوانند تصاویر مجاری صفراوی، کیسه صفرا و عروق و رگهای کبد را بازسازی کنند. استفاده از مواد داخل وریدی حساسیت نتیجه روش را افزایش میدهد، اما هزینهها را نیز افزایش میدهد.
نمونه برداری یا بیوپسی کبد
تنها روش شفاف و روشن برای تشخیص تفاوت رشد سرطان کبد بدخیم یا خوش خیم، بررسی آن با برداشتن نمونهای از بافت و بررسی آن در زیر میکروسکوپ است. به این فرآیند بیوپسی گفته میشود. یک نمونه برداری ممکن است همزمان با سونوگرافی یا سی تی اسکن انجام شود.
لاپاراسکوپی کبدی
در این روش یک جراح ابزاری به نام لاپاراسکوپ (یک لوله نازک و انعطاف پذیر با دوربین و نور در نوک آن) را از طریق یک برش کوچک در شکم در بدن قرار میدهد. لاپاراسکوپی به جراح اجازه میدهد تا مستقیماً به کبد نگاه کند و علائم سرطان کبد را ارزیابی کند.
فناوری DELFI جهت تشخیص زودهنگام سرطانهای کبد
یک فناوری جدید آزمایش خون مبتنی بر هوش مصنوعی که برای تشخیص سرطان ریه در مطالعهای در سال ۲۰۲۱ مورد استفاده قرار گرفته بود اکنون بیش از ۸۰ درصد از سرطانهای کبد را در یک مطالعه جدید شناسایی کرده است.
در این مطالعه ۷۲۴ نفر شرکت داشتند. آزمایش خونی موسوم به «ارزیابی قطعات دیانای برای رهگیری اولیه» به اختصار DELFI DNA Evaluation of Fragments for Early Interception، تغییرات در تجزیه دیانای سلولهای سرطانی که به جریان خون ریخته شده را که با عنوان دیانای بدون سلول(cfDNA) شناخته میشوند، تشخیص میدهد. در جدیدترین مطالعه، محققان از فناوری DELFI بر روی نمونههای پلاسمای خون بهدست آمده از ۷۲۴ فرد در ایالات متحده آمریکا، اتحادیه اروپا و هنگ کنگ برای تشخیص سرطان در سلولهای کبدی استفاده کردند.
محققان بر این باورند که این اولین بررسی تجزیه ژنوم است که به طور مستقل در دو جمعیت پرخطر و در بین گروههای نژادی و قومی مختلف با علل مختلف مرتبط با سرطان کبد انجام شده است. یافتههای آنها در مجله Cancer Discovery و در کنفرانس ویژه انجمن آمریکایی تحقیقات سرطان: پیشگیری دقیق، تشخیص زودهنگام و رهگیری سرطان، گزارش شد. تخمین زده میشود که ۴۰۰ میلیون نفر در سراسر جهان به دلیل سیروز (التهاب شدید) ناشی از بیماریهای مزمن کبدی از جمله هپاتیت ویروسی یا بیماری کبد چرب غیرالکلی، در معرض خطر ابتلا سرطان کبد باشند.
افزایش تشخیص زودهنگام سرطان کبد میتواند جان بسیاری از انسانها را نجات دهد، اما آزمایشهای غربالگری کنونی کمتر مورد استفاده قرار میگیرند و بسیاری از سرطانها را از دست میدهند. از ۷۲۴ نمونه پلاسمای مورد مطالعه، ۵۰۱ نمونه از ایالات متحده و اتحادیه اروپا جمع آوری شد و شامل نمونههایی از ۷۵ نفر مبتلا به سرطان کبد برای آموزش و اعتبارسنجی مدل یادگیری ماشینی بود. این هوش مصنوعی از دادهها و الگوریتمها برای بهبود دقت خود استفاده میکند. برای اعتبارسنجی آن، ۲۲۳ نمونه پلاسمای اضافی متعلق به افراد در هنگ کنگ مورد تجزیه و تحلیل قرار گرفت که شامل نمونههایی از ۹۰ نفر مبتلا به سرطان کبد، ۶۶ نفر مبتلا به ویروس هپاتیت بی، ۳۵ نفر مبتلا به سیروز کبدی مرتبط و ۳۲ نفر عاری از عوامل خطر بود. فناوری DELFI با مطالعه اندازه و مقدار «دیانای بدون سلول» موجود در گردش خون مناطق مختلف ژنوم به بررسی نحوه بستهبندی دیانای در داخل هسته سلول میپردازد.
سلولهای سالم، دیانای را مانند یک چمدان منظم بستهبندی میکنند که در آن نواحی مختلف ژنوم با دقت در محفظههای مختلف قرار میگیرند. در مقابل، هستههای سلولهای سرطانی چمدانهای بینظمتری ایجاد میکنند که مواردی از سراسر ژنوم بهطور تصادفی در آن قرار میگیرد. هنگامی که سلولهای سرطانی میمیرند، قطعات دیانای را به شیوهای آشفته در جریان خون آزاد میکنند. DELFI وجود سرطان را با بررسی میلیونها قطعه از دیانایهای بدون سلول شناسایی میکند.
در این مطالعه جدید، محققان این آزمایش را بر روی قطعات دیانای بدون سلول استخراج شده از نمونههای پلاسما انجام دادند. این آزمایش پیش از این سرطان ریه را به طور دقیق تشخیص داده بود. فناوری DELFI سرطانهای کبد را در مراحل اولیه با حساسیت کلی ۸۸٪ تشخیص داد و تقریباً هرگز نتیجه آن مثبت کاذب نبود. در حال حاضر، کمتر از ۲۰ درصد از جمعیت تحت خطر غربالگری سرطان کبد انجام میدهند. این آزمایش خون جدید میتواند تعداد موارد سرطان کبد شناسایی شده را در مقایسه با آزمایش خون استاندارد موجود، دو برابر کند و تشخیص زودهنگام سرطان را افزایش دهد. محققان در گامهای بعدی قصد دارند این رویکرد را در مطالعات بزرگتر برای استفاده بالینی تأیید کنند. به گفته انجمن سرطان آمریکا، سالانه بیش از ۸۰۰ هزار نفر در سراسر جهان به سرطان کبد مبتلا میشوند و این بیماری یکی از دلایل اصلی مرگ و میر ناشی از سرطان در سراسر جهان است.

تشخیص بهتر سرطان کبد به کمک سیستم بافتبرداری جدید
پژوهشگران روسی، یک سیستم بافتبرداری نوری ابداع کردهاند که میتواند به تشخیص آسانتر سرطان کبد کمک کند. پژوهشگران دانشگاه ایالتی اوریول (Oryol State University) در روسیه، یک سیستم بافتبرداری نوری ابداع کردهاند که میتواند بین بافت سرطانی و سالم کبد تمایز قائل شود. این فناوری جدید میتواند تشخیص سرطان کبد را که ششمین سرطان شایع در جهان است، آسانتر کند.
اوگنی ژربتسوف (Evgenii Zherebtsov)، از پژوهشگران این پروژه معتقد است این فناوری به گونهای طراحی شده است که با سوزنهایی که در حال حاضر برای بافتبرداری کبد استفاده میشوند، سازگار باشد. بدین ترتیب، شاید روزی بتواند به جراحان کمک کند تا دستگاههای بافتبرداری را با دقت بیشتری هدایت کنند و تعداد اشتباهات هنگام برداشتن نمونههای بافت که برای تشخیص استفاده میشوند، کاهش یابد. به گفته پژوهشگران، این سیستم بافتبرداری نوری میتواند به صورت قابل اعتمادی میان سلولهای سرطانی و سالم موشها تمایز قائل شود. همچنین، این سیستم در آزمایشهای ابتدایی انجامشده در افراد مشکوک به سرطان کبد، امیدوارکننده بود.
روشهای بافتبرداری نوری مانند این روش، تشخیص بافتهای سالم و بافتهای دارای تومور را با دقت بالایی ممکن میکند. اگرچه این سیستم به طور خاص برای استفاده در جراحی شکم طراحی شده است اما نتایج پژوهش نشان میدهند که فناوریهای مشابه میتوانند برای سایر کاربردهای پزشکی نیز سودمند باشند.
پژوهشگران، این دستگاه جدید را هنگامی طراحی کردند که جراحان همکار آنها متوجه شدند که انجام دادن بافتبرداری سوزنی دقیقاً در محل مناسب چقدر دشوار است. تشخیص تومورها در مراحل ابتدایی، هنگام وارد کردن یک سوزن توخالی کوچک در کبد برای گرفتن نمونه بافت، دشوار است. اگر سوزن در محل نادرستی قرار داده شود و تومور را از دست بدهد، میتواند تشخیص نادرست را به همراه داشته باشد.
این سیستم بافتبرداری نوری جدید، روش طیفسنجی بازتابی و تصویربرداری از طول عمر فلورسانس (Fluorescence-Lifetime Imaging Microscopy-FLIM) را برای ارزیابی نشانگرهای مرتبط با متابولیسم سلولی که در سلولهای سالم و سرطانی متفاوت است، ترکیب میکند. این کار میتواند به جراحان کمک کند تا محل سرطان را در زمان واقعی ببینند و بتوانند بهترین محل را برای گرفتن نمونه بافت شناسایی کنند. طیفسنجی بازتابی، ویژگیهای بافت را بر اساس نحوه انعکاس نور نشان میدهد. تصویربرداری از طول عمر فلورسانس، بافتها را در معرض طول موجی از نور قرار میدهد که فلورسانس را القا میکند و سپس مدت زمان محو شدن فلورسانس را اندازه میگیرد. زمان فروپاشی فلورسانس، به حضور مولکولهایی بستگی دارد که در متابولیسم مهم هستند.
اگرچه این گروه و سایر گروههای پژوهشی، پیشتر از شدت فلورسانس برای ارزیابی بافت استفاده کردهاند اما بررسیهای انجام شده در سایر قسمتهای بدن نشان دادهاند که طول عمر فلورسانس، کمتر به شرایط آزمایشی وابسته است. اندازهگیریهای طول عمر فلورسانس در حضور خون و زمانی که نور یکنواخت وجود ندارد یا در صورت تغییر تماس میان کاوشگر و بافت به دلیل حرکت، ثابتتر باقی میماند. پژوهشگران با تمرکز بر استفاده از ابزار جدید برای بافتبرداریهای آینده، عناصر فشرده و جدیدی را برای دستگاه انتخاب کردند. کاوشگری به قطر یک میلیمتر، با سوزن استاندارد بافتبرداری سازگار است و کانالهای نوری مجزایی برای طیفسنجی بازتابی و اندازهگیری طول عمر فلورسانس دارد.
انتقال کاوشگر به مراکز درمانی
پژوهشگران برای ارزیابی حساسیت این سیستم، ابتدا محلولهای شناخته شده حاوی مولکولهایی را که نقش کلیدی در متابولیسم دارند، اندازه گیری کردند. آنها پس از به دست آوردن نتایج رضایتبخش، آزمایشهایی را در موشهای مبتلا به سرطان کبد و بیماران مشکوک به سرطان کبد انجام دادند. پژوهشگران دریافتند که ابزار آنها و پارامترهایی که اندازهگیری کردهاند، به طور قابل اعتمادی میتوانند بافت مبتلا به سرطان کبد و بافت کبد سالم را تشخیص دهند.
بررسیها روی بیمارانی که توموری مشابه تومور موشها داشتند، نشان داد که این روش میتواند نتایج پایدار و قابل تکراری را ارائه دهد که میتوان از آنها برای تشخیص سرطان استفاده کرد. پژوهشگران قصد دارند به اندازهگیری پارامترهای طول عمر فلورسانس در بیماران مبتلا به انواع گوناگون تومور در مراحل مختلف ادامه دهند تا عوامل طبقهبندیکننده فوری را تولید کنند. همچنین، این کار میتواند استفاده از روشهای پیشرفته یادگیری ماشینی را که به جراحان در تصمیمگیری بالینی طی بافتبرداری کمک میکنند، ممکن کند. این پژوهش، در مجله Biomedical Optics Express به چاپ رسید.

امواج فراصوت جهت ریشه کنی سرطان کبد در موشها
دانشمندان آمریکایی موفق شدند با استفاده از امواج صوتی غیر تهاجمی، سرطان کبد را در موشها ریشه کن کنند. در این روش نوین، موشهای مبتلا به سرطان کبد، نوعی اثربخشی را در زمینه درمان با امواج صوتی غیرتهاجمی از خود نشان دادند. در این تحقیقات، محققان آمریکایی از امواج فراصوت (اولتراسوند) برای تخریب ۷۵ درصد از حجم یک تومور کبد استفاده کردند. به نظر میرسد این روش درمانی سبب میشود تا سیستم ایمنی موشها تحریک شده و باقی بافتهای سرطانی را خود پاکسازی کند. محققان این پژوهش معتقد هستند در ۸۰ درصد از موارد، به نظر میرسید سرطان از بین رفته است و هیچ نشانهای از متاستاز و یا عود کردن بیماری در سه ماهی که این موشها تحت نظر بودند، وجود نداشت.
این درمان که «هیستو تریپسی» نام دارد، در حال حاضر در حال آزمایش بر روی انسانهای مبتلا به سرطان کبد است. یکی از افراد فعال در زمینه مهندسی پزشکی از دانشگاه میشیگان آمریکا در توضیح این مسأله گفت: هیستوتریپسی یک انتخاب امیدوارکننده است که میتواند بر محدودیت روشهای فعلی ریشه کن کردن بافتهای سرطانی غلبه کرده و نوعی روش ایمن و مؤثر به شیوه غیر تهاجمی برای ریشه کن کردن تومور کبد ارائه دهد. محققان امیدوارند فراگیری این پژوهش، سبب تحقیقات بیشتر در زمینه پیش بالینی و بالینی هیستوتریپسی برای دست یابی به هدف نهایی اتخاذ این روش درمانی برای بیماران مبتلا به سرطان کبد شود.
افزایش طول عمر بیماران مبتلا به سرطان کبد
محققان شیوه درمانی جدیدی برای سرطان کبد ابداع کردهاند که رشد تومور را به میزان قابل توجهی کاهش و طول عمر مبتلایان به این بیماری را به میزان چشمگیری افزایش میدهد. در این شیوه جدید از فناوری حذف با بسامد رادیویی (RFA) به همراه یک داروی شیمی درمانی موسوم به Sunitinib استفاده میشود. با وجود این که هریک از روشهای مذکور به تنهایی تا حدی بر درمان سرطان کبد تأثیر دارند، ترکیب این دو شیوه با هم موجب بروز یک واکنش سیستم ایمنی قوی و نابودسازی سلولهای سرطانی میشود.
در تحقیقات محققان دانشگاه میسوری در آمریکا که با استفاده از موشها انجام شد، موشهای مبتلا به سرطان کبد ابتدا با داروی Sunitinib تحت درمان قرار گرفتند تا توانایی سلولهای سرطانی در گریز از سیستم ایمنی کاهش یابد. سپس از فناوری RFA به عنوان محرکی برای ایجاد واکنش سیستم ایمنی بدن در برابر تومور سرطانی استفاده شد. در نتیجه این اقدام، سرعت رشد تومور به میزان قابل توجهی کاهش یافت و طول عمر موشهای تحت درمان با این شیوه نیز افزایش چشمگیری یافت.
مطالعات محققان دانشکده پزشکی دانشگاه هاروارد نیز نشان میدهد مصرف انواع سبزیجات، گریپ فروت، گردو، لیمو، آووکادو، چای سبز، سیر، چغندر، سبزیجات با برگهای سبز پررنگ و زردچوبه مهمترین غذاهایی هستند که کبد را سالم نگه میدارند. در ادامه نتایج این تحقیقات آمده است که استفاده از غذاهای آماده و حاضری، الکل و سیگار، روغن و غذاهای سرخ کرده و بیتحرکی مهمترین دلایل آسیب به کبد هستند. گزارش کامل این تحقیقات در نشریه Journal for ImmunoTherapy of Cancer منتشر شده است.
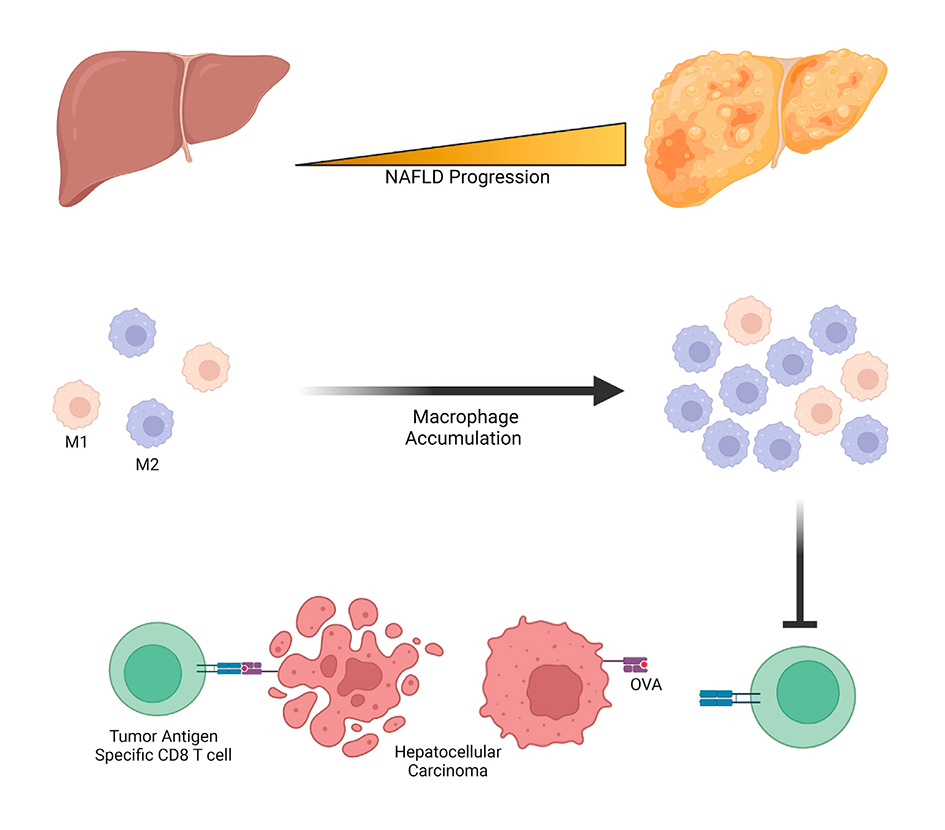
تولید سلولهای T مهندسی شده رویکردی جدید در درمان سرطان کبد
آلودگی با ویروس هپاتیت B به عنوان یک اپیدمی خاموش به حساب میآید، زیرا افراد مبتلا هیچ علامتی ندارند و به صورت ناخودآگاه ویروس را به دیگران منتقل میکنند. علائم عفونت ویروس هپاتیت سالها پس از عفونت اولیه ظاهر میشود و متاسفانه بسیاری از بیماران با ابتلا به سرطان کبد به نام کارسینوم سلولهای کبدی یا HCC مراجعه میکنند. در این مرحله حساس، پیوند کبد بهترین رویکرد درمانی برای بیماران است. با این حال، آثار HBV در قسمتهای دیگر بدن همچنان پابرجاست که در کنار استفاده از رژیم مادام العمر داروهای سرکوب کننده سیستم ایمنی در این بیماران که برای مهار سیستم دفاعی بدن و جلوگیری از رد اندام اهدا کننده صورت میگیرد منجر به گسترش سلولهای سرطانی در کبد تازه پیوندی میشود. در حال حاضر درمانهای سلولی با استفاده از سلولهای T مهندسی شده به صورت بالینی در دسترس است، سلولهای ایمنی بیمار جهت هدف قرار دادن و از بین بردن سلولهای تومور دستکاری میشوند. با این حال، استفاده از داروهای سرکوب کننده سیستم ایمنی در این بیماران اثر درمانی سلولهای T را کاهش داده و منجر به مرگ آنها میشود.
تیمی به سرپرستی آنتونیو برتولتی از شبکه ایمونولوژی سنگاپور موفق به تولید سلول T مهندسی شدهای شدند که در برابر داروهای سرکوب کننده سیستم ایمنی مقاوم هستند. این سلولهای T منحصر به فرد به گونهای دستکاری ژنتیکی شدهاند که سلولهای سرطانی کبد که دارای قطعاتی از پروتئین HBV هستند را تشخیص داده و هدف قرار میدهند. این سلولها میتوانند تواناییهای خود در از بین بردن سلولهای سرطان را حتی در حضور داروهای سرکوب کننده سیستم ایمنی حفظ کنند. این کشف راه را برای گروه جدیدی از درمانهای مبتنی بر سلول T برای بیماران مبتلا به HCC با HBV مثبت باز میکند که میتوانند به طور اختصاصی تومورها را از بین ببرند در حالی که بافتهای سالم کبد را دست نخورده میگذارند.
درمان نوع تهاجمی سرطان کبد با کمک یک روش پرتودرمانی
پژوهشگران استرالیایی سعی دارند با کمک یک روش پرتودرمانی، به درمان یک نوع تهاجمی از سرطان کبد کمک کنند. آزمایش پرتودرمانی موسوم به SABR، یک روش غیرتهاجمی است که امکان ارسال دقیق دوزهای بالایی از پرتوها را فراهم میکند. در حال حاضر برای درمان کارسینوم هپاتوسلولار که رایجترین نوع سرطان کبد است، یک درمان حرارتی به کار میرود که در آن از دمای شدید برای برداشتن تومور سرطانی استفاده میشود و درمان مستقیماً با استفاده از سوزن به تومور وارد میشود. مراقبت همیشه موفقیتآمیز نیست زیرا سرطان در بیش از ۳۰ درصد موارد ممکن است دوباره رخ دهد و تعدادی از افراد به دلیل اندازه تومور، در وهله اول نمیتوانند به درمان دسترسی داشته باشند.
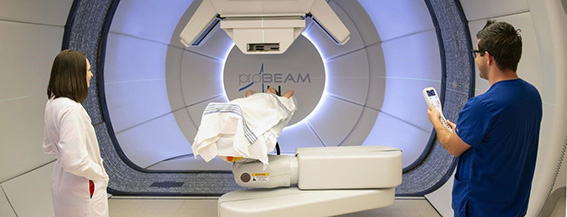
از سوی دیگر، پرتودرمانی SABR، یک روش پرتودرمانی نسبتاً جدید است که پیشتر با موفقیت برای درمان تعدادی از سرطانهای دیگر استفاده شده اما هنوز به طور گسترده برای درمان سرطانهای کبد مورد استفاده قرار نگرفته است. این روش غیرتهاجمی به واسطه هدف قرار دادن تومور با پرتوها از زوایای گوناگون انجام میشود که امکان ارائه دوز بالا، درمان دقیق و کاهش آسیب به بافتهای سالم اطراف را طی سه تا پنج جلسه فراهم میکند. این پروژه که با همکاری متخصصان برجسته خونشناسی، پرتودرمانی و رادیولوژیستها در ۱۶ مرکز درمان کبد استرالیا انجام میشود، یک بررسی تصادفی و کنترلشده را برای مقایسه درمان غیرتهاجمی با استانداردهای کنونی انجام خواهد داد و ممکن است بتواند به تغییر درمان کمک کند. در حال حاضر، روش SBRT، یک روش تجربی در نظر گرفته میشود و تنها زمانی مورد استفاده قرار میگیرد که درمانهای صف اول شکست بخورند. با وجود این، بررسیهای ابتدایی نشان دادهاند که این درمان میتواند با عوارض جانبی بسیار کم به کنترل تومورها بپردازد و به مواردی برسد که به دلیل اندازه تومور یا محل قرار گرفتن آن، قابل درمان نیستند. پژوهشگران میگویند که با افزایش میزان سرطان کبد در سراسر استرالیا، بسیار مهم است که بهترین درمان اثبات شود و مورد استفاده قرار بگیرد. میزان سرطان کبد در ۳۰ سال گذشته افزایش یافته است که دومین افزایش قابل توجه در میان انواع سرطان به شمار میرود. این در حالی است که میزان مرگ و میر ناشی از این سرطان، بیشترین افزایش را در بین سرطانها داشته است.
کارسینوم هپاتوسلولار، سرطانی با احتمال کم زنده ماندن بیمار به شمار میرود که با شیوع سریع در حال افزایش است. بنابراین، یافتن راهی برای بهبود نتایج درمان در بیماران حیاتی است.
روش SABR میتواند کنترل تومور را بهبود ببخشد. توانایی آن برای ارائه به صورت سرپایی و در جلسات درمانی کمتر به این معنی است که احتمالاً مقرون به صرفه است و میتواند به سرعت در عمل بالینی به کار گرفته شود. این آزمایش پنج ساله، در همه ایالتهای اصلی استرالیا آغاز شده است.
مادهای جدید برای درمان سرطان کبد
موسسه مهندسی بیومدیکال Suzhou تحت نظارت آکادمی علوم چین به تازگی اعلام کرده است این محققان نوعی ماده نانومتری تولید کردهاند که میتوان از آن برای درمان سرطان کبد استفاده کرد.
به گفته محققان، این ماده که در کنار پرتو درمانی مورد استفاده قرار میگیرد، روشی مؤثر و ایمن برای درمان این نوع سرطان است.
پرتو درمانی که روشی استاندارد برای معالجه سرطان است، نقش مهمی در روند درمان این بیماری دارد اما با این حال برخی از انواع تومورهای سرطانی جامد، نسبت به این روش درمان مقاوم بوده و در نتیجه این بافتهای سرطانی با پرتو درمانی قابل معالجه نخواهند بود. در چنین مواقعی سلولهای سرطانی شانس بقا پیدا کرده و احتمال عود کردن بیماری وجود دارد. مدتهاست محققان به دنبال روشی برای مقابله با این تومورهای مقاوم هستند تا بتوانند آنها را بهطور کامل ریشهکن کنند. در حال حاضر، متخصصان چینی در این موسسه موفق به ساخت نوعی نانوذرات از جنس سیلیسیم دیاکسید و طلا شدند که حدود ۲۰۰ نانومتر طول و ۱۰۰ نانومتر عرض دارند.
این نانوذرات از طریق تزریق وریدی وارد بدن میشوند و به بافت سرطانی میرسند. همچنین این ذرات حامل نوعی داروی ضد سرطان هستند و این دارو را به سلولهای تومور منتقل میکنند. آزمایشهای انجام شده روی موشها نشان داده است که استفاده از نانوذرات جدید در روند درمان، حساسیت تومورها را به پرتو درمانی افزایش داده و میتواند با آنها به شیوهای موثرتر مقابله کند. همچنین وجود نانو ذرات طلا به همراه داروی ضد سرطان، قدرت مقابله این نانوذرات با سلولهای سرطانی را افزایش میدهد. جزئیات بیشتر این تحقیق در مجله Applied Materials and Interfaces چاپ انجمن شیمی آمریکا منتشر شده است.
منابع:
https://bonyannews.ir
https://aftabnews.ir
https://maysa-lab.com
دیدگاه ها