
به منظور بهبود تشخیص در بیماران، نرم افزارهای پردازش تصویر مختلفی برای استخراج اطلاعات مفید از تصاویر پزشکی ارائه شدهاند. متخصص خون، مطالعه میکروسکوپی خون انسان را انجام میدهد که به روشهایی از جمله تصویربرداری رنگی میکروسکوپ، تقسیم بندی، طبقه بندی و خوشه بندی نیاز دارد و میتوانند بیماران مبتلا به سرطان خون را شناسایی کنند. سرطان خون با گلبول سفید خونی بلاست (WBC) مرتبط است. ماهیت غیر اختصاصی علائم و نشانههای ALL (لوسمی حاد لنفاوی) اغلب منجر به تشخیص نادرست میشود بنابراین متخصص خون نیز برای طبقه بندی سلولهای بلاست دچار مشکل میشود و از طرف دیگر طبقه بندی دستی سلولهای خون زمان بر و مستعد خطا است. بنابراین شناسایی سریع، دقیق و خودکار سلولهای مختلف خون مورد نیاز است. در این مقاله جهت تقسیم بندی سلولهای خونی، روش خودکار آستانهگذاری Otsu همراه با افزایش کیفیت تصویر و محاسبات برای تقسیم بندی WBC ارائه شده است. برای طبقه بندی و تشخیص سلولهای بلاست از سلولهای لنفوسیت نرمال از طبقه بندی کننده kNN استفاده شده است. این سیستم بر روی 108 تصویر موجود در مجموعه عمومی دادههای تصویر برای مطالعه سرطان خون اعمال شده است. این روش دارای دقت 93٪ است.
۱. مقدمه
لوسمی، سرطان خون مرتبط با گلبولهای سفید خون است. این یک اختلال در مغز استخوان است که هنگام خود تکثیری مداوم گلبولهای سفید غیر طبیعی خون ایجاد میشود. این سلولها عملکرد طبیعی ندارند، عملکردی که برای مقابله با عفونتها لازم است. با تجمع آنها از تولید سلولهای خونی نرمال دیگر در مغز استخوان جلوگیری شده و منجر به کم خونی، خونریزی و عفونتهای مکرر میشود. با گذشت زمان، سلولهای لوسمی از طریق جریان خون در جایی که تقسیم شدن را ادامه دهند، پخش میشوند و گاهی اوقات تومور ایجاد کرده و به اندامهایی مانند کلیه و کبد آسیب میرسانند. سرطان خون حاد بر اساس طبقه بندی فرانسوی-آمریکایی- بریتانیایی (FAB) به دو نوع سرطان خون لنفوبلاستیک حاد (ALL) و سرطان خون میلوژن حاد (AML) طبقه بندی میشود. سرطان خون حاد نوعی بیماری است که به سرعت در حال پیشرفت است و بیشتر سلولهایی که شکل نگرفتهاند را تحت تأثیر قرار میدهد (هنوز کاملاً رشد نکرده و تمایز نیافتهاند). ALL بیشتر در کودکان شایع است در حالی که AML عمدتاً بزرگسالان را درگیر میکند اما ممکن است در کودکان و نوجوانان نیز رخ دهد. در سال 2009 تخمین زده شده است که تقریباً 31490 نفر مبتلا به سرطان خون بوده و 44510 نفر در ایالات متحده بر اثر این بیماری خواهند مرد. شناسایی زودهنگام و سریع نوع سرطان خون، کمک شایانی به ارائه درمان مناسب برای نوع خاص آن میکند. تشخیص آن با شمارش کامل خون (CBC) شروع میشود. اگر شمارش غیر طبیعی باشد، به بیمار پیشنهاد میشود تا از مغز استخوان نمونه برداری انجام دهد. بنابراین برای تأیید حضور سلولهای سرطانی، مطالعه مورفولوژی (ریخت شناسی) مغز استخوان و آنالیز اسلاید خون محیطی انجام میشود. به منظور طبقه بندی سلولهای غیر طبیعی در انواع خاص آنها و زیرگروه سرطان خون، یک متخصص خون برخی سلولها را زیر میکروسکوپ نوری برای یافتن ناهنجاریهای موجود در هسته یا سیتوپلاسم سلولها مشاهده میکند. رفتار بالینی بیماری را میتوان با استفاده از این طبقه بندی پیش بینی کرد و بر همین اساس، درمان باید به بیمار ارائه شود. در بیماری سرطان خون، تعداد زیادی گلبول سفید غیر طبیعی به دلیل نامعلومی توسط مغز استخوان تولید میشوند. در آسیب شناسی، تشخیص دستی لوسمی انجام میشود که به دلیل هزینه بالای ابزار آسیب شناسی، زمان بر و همچنین هزینه بر است. از این رو روش اتوماتیک برای نتایج سریع و دقیق به کار گرفته میشود. در این روش، تصویر نمونه خون پردازش میشود و قسمت هسته آن جدا شده و در نهایت سلولها به انواع بلاست و نرمال دستهبندی میشوند.
۲. سیستم تشخیص لوسمی حاد
این شامل ماژولهای عملکردی مختلف است. دو مرحله اصلی مطرح شده در این سیستم، تقسیم بندی و طبقه بندی تصویر هستند. تصویر ورودی اسلاید خون به سیستم داده میشود. خون دارای چهار عنصر اصلی یعنی گلبولهای قرمز، گلبولهای سفید، پلاکتها و پلاسما است تا عملکرد درست و کاملی داشته باشد.

شکل ۱. بلوک دیاگرام یک سیستم طراحی شده
ترکیب و غلظت گلبولهای سفید خون، دارای اطلاعات ارزشمندی است و نقشی اساسی در تشخیص بیماریهای مختلف دارد. از این رو اولین ماژول در سیستم طراحی شده، شناسایی گلبول سفید خون است. گلبولهای سفید در پنج گروه نوتروفیل، ائوزینوفیل، بازوفیل، مونوسیت و لنفوسیت قرار میگیرند. رشد غیر قابل کنترل لنفوسیت، دلیل ایجاد سرطان خون است. بنابراین سلولهای لنفوسیت در میان گلبولهای سفید خون با تقسیم بندی شناسایی میشوند. سپس ویژگیهای لنفوسیتها از قبیل مساحت، محیط، دواری، ضخامت و غیره استخراج میشود. سپس این ویژگیها به ماژول طبقه بندی کننده اعمال میشوند که در آن طبقه بندی بین سلولهای نرمال و سلولهای بلاست انجام شده و لوسمی تشخیص داده میشود. متداولترین روش برای طبقه بندی سرطان خون روش FAB است. امروزه این روش با طبقه بندی ایمونولوژیک (ایمنی شناسی) که مبتنی بر تصویر نیست به روزرسانی شده است. از طرف دیگر، روش FAB هنوز هم برای طبقه بندی مورفولوژیکی مبتنی بر تصویر، معتبر است. برای طبقه بندی از طبقه بندی کنندههای مختلفی مانند خطی، kNN، فازی (fuzzy) و غیره استفاده میشود.
۳. بررسی تقسیم بندی تصویر
تقسیمبندی به معنی تجزیه تصویر به بخشهای مختلف برای کاربردهای مختلف است. مرحله تقسیم بندی بسیار مهم است زیرا دقت در استخراج و طبقه بندی ویژگی بعدی به تقسیم بندی صحیح گلبولهای سفید بستگی دارد. همچنین به دلیل ماهیت پیچیده سلولها و عدم اطمینان در تصویر میکروسکوپی، این مسئله یک مشکل دشوار و چالش برانگیز است. بنابراین این مرحله مهمترین چالش در بسیاری از مقالات است و بهبود تقسیم بندی سلولی، رایجترین اقدام در بسیاری از کارهای پژوهشی بوده است. بسیاری از محققان روشهای مختلفی را برای تقسیم بندی تصویر ارائه دادهاند؛ مانند روشهای مبتنی بر آستانه گذاری، مبتنی بر لبه، مبتنی بر منطقه یا خوشه بندی مثل خوشه بندی میانگین fuzzy-C و خوشه بندی K- میانگین.
Cseke از روش آستانه گذاری خودکار استفاده کرد (سال 1979). روشهای آستانه همیشه نمیتوانند نتایج معنی داری داشته باشند زیرا از هیچ اطلاعات مکانی هنگام انتخاب آستانه تقسیم بندی استفاده نمیشود. آنها اغلب با عملیات مورفولوژی ریاضی ترکیب میشوند. این روش 92٪ صحیح بود. لیائو یک روش تقسیم بندی دقیق برای گلبولهای سفید خون ارائه میدهد. یک روش آستانه گذاری ساده برای اختصاص دادن برچسبهای اولیه به پیکسلها در تصاویر سلولهای خونی اعمال میشود. این الگوریتم بر اساس اطلاعات پیشین درباره تصاویر لام خون است. سپس برچسبها با استفاده از یک روش تشخیص شکل مبتنی بر اطلاعات زمینه منطقهای گسترده تنظیم میشوند تا به نتایج مفیدی برسند. این طرح تنها در صورتی مناسب است که شکل لایه مرزی هر گلبول سفید نزدیک به یک دایره باشد. روش تشخیص لبه نیز میتواند برای تقسیم بندی مفید باشد اما فقط در مواردی که کنتراست خوبی بین پیشزمینه و پسزمینه وجود داشته باشد، قابل استفاده است. Piuri و Scotti و S. H. Rezatofighi و همکاران، تقسیم بندی هسته گلبولهای سفید را بر اساس فرایند متعامد سازی گرام-اشمیت، برای تقویت بردارهای رنگی مورد نظر ارائه دادهاند. Jiang و همکاران با ترکیب دو روش، فیلتر کردن فضای مقیاس و خوشهبندی watershed، روش تقسیمبندی جدیدی برای گلبولهای سفید ارائه دادند. در این طرح، دو جز گلبول سفید، هسته و سیتوپلاسم، به ترتیب با استفاده از روشهای مختلف استخراج میشوند. ابتدا یک تصویر فرعی حاوی WBC از تصویر سلول جدا میشود. سپس، از فیلتر کردن فضای مقیاس برای استخراج ناحیه هسته از تصویر فرعی استفاده میشود. بعد از آن، خوشه بندی watershed در هیستوگرام سه بعدی HSV (رنگ، اشباع، مقدار) برای استخراج ناحیه سیتوپلاسم پردازش میشود. سرانجام، عملیات مورفولوژی برای به دست آوردن کل طرح یکپارچه با موفقیت انجام میشود که از تنوع و پیچیدگی در فضای تصویر جلوگیری میکند و میتواند قسمتهای مختلف WBC را از تصاویر لام خون محیطی استخراج کند. روش خوشه بندی K- میانگین توسط Sinha و Ramakrishnan برای تعیین محل هستههای گلبولهای سفید برای شناسایی گلبولهای سفید روی تصویر، پس از عمل برش زدن برای جداسازی کل سلول از تصویر استفاده میشود. با این حال، روش برش کل سلول به منظور به دست آوردن مساحت واقعی تمام سلول به وضوح نشان داده نشده است. Theera-Umpon از خوشه بندی C-Mean فازی برای تقسیم تصاویر تک سلولی سلولهای سفید خون در مغز استخوان به دو ناحیه یعنی؛ هسته و غیر هسته استفاده کرد. اگر تعداد خوشهها بیشتر از دو عدد باشند، زمان محاسبات افزایش مییابد.
4- الگوریتم تقسیم بندی تصویر
روش مطرح شده برای تقسیم بندی سلولهای خونی (لکوسیتها) در زیر آورده شده است:
مرحله 1: تصویر رنگی اسلاید خون را به سیستم وارد کنید.
مرحله 2: تصویر رنگی را به تصویر سیاه-سفید تبدیل کنید.
مرحله 3: کنتراست تصویر سیاه- سفید را با روش هموارسازی هیستوگرام افزایش دهید (A).
مرحله 4: برای تنظیم سطح شدت (نور) تصویر، کنتراست خطی را به تصویر سیاه- سفید بسط دهید (B).
مرحله 5: تصویر I1 = B + A را برای روشن شدن سایر اجزای تصویر به جز هسته سلول به دست آورید.
مرحله 6: تصویر I2 = I1-A را برای مشخص کردن کل اجزای تصویر به همراه هسته سلول به دست آورید.
مرحله 7: تصویر I3 = I1 + I2 را برای حذف سایر اجزای خون با حداقل اثر تحریف و تغییر شکل بر روی هسته به دست آورید.
مرحله 8: برای کاهش نویز، لبهها را حفظ کرده و تیرگی هسته را افزایش دهید و فیلتر حداقل 3 در 3 را روی تصویر I3 اعمال کنید.
مرحله 9: روش آستانه گذاری جهانی Otsu را روی تصویر I3 اعمال کنید.
مرحله 10: با استفاده از مقدار آستانه در مرحله فوق، I3 را به تصویر باینری تبدیل کنید.
مرحله 11: برای حذف گروههای پیکسل کوچک از دریچه مورفولوژی استفاده کنید.
مرحله 12: برای تشکیل اجزا، پیکسلهای مجاور را به هم متصل کنید.
مرحله 13: با استفاده از تست اندازه، همه اجزایی که کمتر از 50٪ میانگین مساحت RBC هستند، حذف میشوند. مشاهده شده است که این روش تقسیم بندی نسبت به روشهای قبلی نتایج بهتری به دست داده است.
5- استخراج ویژگی
استخراج ویژگی به معنای انتقال دادههای ورودی به مجموعه ویژگیهای مختلف است. در پردازش تصویر، این یک روش برای تعریف مجدد مجموعه بزرگی از دادههای زائد به مجموعهای از ویژگیها (یا بردار ویژگی) با ابعاد کاهش یافته است. در این مقاله سه ویژگی سلولهای لنفوسیت یعنی مساحت، محیط و دواری مشاهده شده است زیرا شکل هسته از ویژگیهای مهم برای متمایزسازی بلاستها است. تمام ویژگیها از تصویر معادل باینری هسته با پیکسلهای غیر صفر نشان دهنده ناحیه هسته استخراج میشوند.
مساحت: مساحت با شمارش تعداد کل پیکسلهای غیر صفر در ناحیه تصویر تعیین شد.
محیط: با محاسبه فاصله بین پیکسلهای مرزی متوالی اندازه گیری شد.
دواری: این یک پارامتر بدون بعد است که با بینظمیهایی سطح تغییر میکند و به صورت زیر تعریف میشود:

6- طبقه بندی
بر اساس ویژگیهای استخراج شده در مرحله فوق طبقه بندی کننده، سلولهای لنفوسیت را به سلولهای بلاست یا نرمال طبقهبندی میکند. طبقه بندی، کار اختصاص دادن برچسبی از یکی از کلاسهای شناخته شده به بردار آزمون ناشناخته است. قاعده تصمیمگیری K- نزدیکترین همسایه (kNN) یک ابزار طبقه بندی رایج با انطباقپذیری خوب بوده است. تجربه گذشته نشان داده است که انتخاب بهینه K به دادهها بستگی دارد و تنظیم پارامتر را برای برنامههای مختلف دشوار میکند. K- نزدیکترین همسایه (kNN) یک روش طبقه بندی غیر پارامتری است. این روش، ساده اما در موارد زیادی بسیار مؤثر است. در اینجا همچنین از kNN برای طبقهبندی سلولهای بلاست از گلبولهای سفید نرمال استفاده شده است.
7- پایگاه داده
به منظور مطالعه، مجموعه دادههای تصویری تحت نظارت عمومی (ALL-IDB) توسط Fabio Scotti برای آزمایش و مقایسه منصفانه الگوریتمها جهت تقسیم بندی و طبقه بندی سلولی بیماری ALL ارائه شده است. دو نوع مجموعه داده در دسترس است. ALL-IDB1 میتواند برای آزمودن قابلیت تقسیم بندی الگوریتمها و همچنین سیستمهای طبقه بندی و روشهای پیشپردازش تصویر مورد استفاده قرار گیرد وALL-IDB2 ، گلبولهای سفید را برای آزمودن طبقه بندی سلولهای بلاست تقسیم بندی کرده است. نمونههای تصاویر مجموعه داده ALLIDB1 در شکل 2 نشان داده شده است.
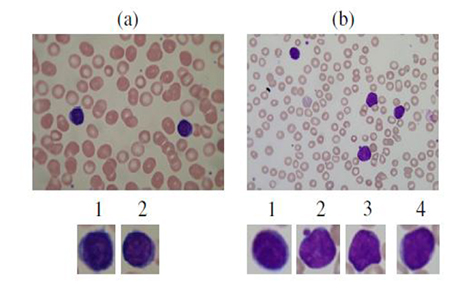
شکل 2. نمونههای تصاویر خون سالم (a)، خون با بلاستهای ALL(b). (a1-2) و (b1-4) زیرمجموعههای بزرگنمایی شده تصاویر (a) و (b) به ترتیب متمرکز شده بر لنفوسیتها و لنفوبلاست هستند.
8- نتایج تجربی
روش پیشنهادی بر روی 108 تصویر لام خون محیطی به دست آمده از مجموعه داده عمومی که قبلاً ذکر شد، اعمال شد. یک تصویر خون میکروسکوپی با اندازه 2592 × 1944 برای ارزیابی در نظر گرفته شده است. همانطور که در بخش ۴ ذکر شد، الگوریتم روی تصویر ورودی اعمال شد. تصاویر حاصل از تقسیم بندی در شکلهای 3، 4، 5 و 6 نشان داده شدهاند.

شکل ۳. تصویر اصلی

شکل ۴. گلبولهای سفید خون با لکههای سفید روی هسته

شکل ۵. تصویر تقسیم بندی شده نهایی
در نتیجه تعداد WBC ها نیز محاسبه میشود. در شکل ۳ آنچنان که نشان داده شده، تعداد WBC های موجود 11 است. WBC ها با لکههای سفید روی هسته از سایر اجزای خون جدا میشوند. در تصویر تقسیم بندی شده نهایی با از بین بردن تمام اجزای نویزدار با کمترین فیلتر، تنها WBC ها با هسته تیرهتر باقی میمانند. بعد از این تقسیم بندی، سلولهای لنفوسیت توسط تقسیم بندی بلاست و ویژگیهای لنفوسیت محاسبه شده، از بین همه WBC ها شناسایی میشوند. بسته به ویژگیهای مورفولوژی، این تصمیم گرفته میشود که آیا این تصویر اسلاید لوسمی است یا خیر. تصویر بلاست لنفوسیت جدا شده نهایی در شکل ۶ نشان داده شده است.

شکل ۶. تصویر بلاست لنفوسیت جدا شده. این روش روی همه ۱۰۸ تصویر اعمال میشود. دقت این روش 93٪ بود.
9- نتیجه
هدف اصلی این مقاله تقسیم بندی تصویر اسلاید خون و به دنبال آن استخراج ویژگی برای تشخیص لوسمی است. ویژگیهای شکل هسته مانند مساحت، محیط، دواری و غیره برای دقت بهتر تشخیص در نظر گرفته میشوند. تشخیص لوسمی با ویژگیهای مطرح شده با استفاده از طبقه بندی kNN دارای دقت کلی 93٪ است. علاوه بر این، این سیستم باید نسبت به رنگ آمیزی (لکه گذاری) بیش از حد سلول و لمس آن مقاوم باشد. نتایج به دست آمده، کارهای آینده را از جمله برای طبقه بندی لنفوبلاست به انواع مختلف ترغیب میکند. روشهای جایگزین را میتوان برای تقسیم بندی تصویر لکه خون مستقل از رنگ و طبقه بندی نوع لوسمی بررسی کرد.
منابع:
[1] Catherine Haworth, Ad Heppleston, Ph Morris Jones, Rha Campbell, Dik Evans, Mk Palmer, From the Royal Manchester Children’s Hospital, Pendlebury, Manchester M27 JHA, and the *Department of Statistics, Christie Hospital and Holt Radium Institute, Withington, Manchester M20 9BX, “Routine bone inarrow examination in the management of acute lymphoblastic leukaemia of childhood”, J Clin Pathol 1981 ;34:483-485.
[2] Hayan T. Madhloom1, Sameem Abdul Kareem 2, Department of Artificial Intelligence, Faculty of Computer Science and Information, “A Robust Feature Extraction and Selection Method for the
Recognition of Lymphocytes versus Acute Lymphoblastic Leukemia”, International Conference
on Advanced Computer Science Applications and Technologies, 2012.
[3] Ruggero Donida Labati IEEE Member, Vincenzo Piuri IEEE Fellow, Fabio Scotti IEEE Member, University of degli Studi di Milano, Department of Information Technologies, via Bramante 65, 26013 Crema, Italy, “ALL-IDB: The Acute Lymphoblastic Leukemia Image Database For Image Processing”, 2011 IEEE.
[4] Wei-Liang Tai, Department of Biomedical Informatics, Asia University, Taiwan, “Blood Cell
Image Classification Based on Hierarchical SVM”, 2011 IEEE.
[5] Waidah Ismail, Department of Information Systems, Computing and Mathematics, Brunel University, “Automatic Detection And Classification Of Leukemia Cells”, June 2012.
[6] Mostafa Mohamed, Behrouz Far, Department of Electrical and Computer Engineering, University of Calgary, Calgary, Canada, “An Enhanced Threshold Based Technique for White Blood Cells Nuclei Automatic Segmentation”, 14th International Conference on e-Health Networking, Applications and Services 2012.
[7] Cseke, I., Geometry GIS System House Ltd. Budapest 1025, Felso Zoldmali 128-1 30. Hungary “A fast segmentation scheme for white blood cell images”, Proceedings of the 11th IAPR International Conference on Pattern Recognition Image, Speech and Signal Analysis, Aug. 30-Sept. 1992, Netherlands, pp: 530-533.
[8] Qingmin Liao, Yingying Deng, Department of Electronic Engineering, Tsinghna University,
P.R.China, “An Accurate Segmentation Method for White Blood Cell Images”, 0-7803-7584-x/OU$17.00 @ 2002 IEEE.
[9] Vincenzo Piuri, Fabio Scotti University of Milan, Department of Information Technologies, via
Bramante 65, 26013 Crema, Italy, “Morphological Classification of Blood Leucocytes by Microscope Images”, CIMSA 2004 -IEEE lntemational Conference on Computationvl Intelligence far Memrement Systems and Applications Boston, MA. USA, 14-16 July 2004.
[10] S. H. Rezatofighi, Control and Intelligent Processing Center of Excellence, University of Tehran, Tehran, Iran, “A New Approach to White Blood Cell Nucleus Segmentation Based on Gram-Schmidt Orthogonalization”, International Conference on Digital Image Processing, IEEE 2009.
[11] Jiang, K., Q.X. Jiang and Y. Xiong, Tsinghua University, Beijing, “A novel white blood cell
segmentation scheme using scale-space filtering and watershed clustering” Mach. Learning Cybernetics, 5: 2820-2825, Proceedings of the Second International Conference on Machine Learning and Cybernetics, xi”, 2-5 November 2003.
[12] Neelam Sinha and A. G. Ramakrishnan, Department of Electrical Engineering Indian Institute of Science Bangalore, “Automation of Differential Blood Count”, 2003 IEEE.
[13] Nipon Theera-Umpon, Electrical Engineering Department, Chiang Mai University, Chiang Mai, Thailand, “Breast Abnormality Detection in Mammograms Using Fuzzy Inference System”, The International Conference on Fuzzy Systems 2005 IEEE.
[14] H.T. Madhloom, S.A. Kareem, University of Malaya, Malaysia, “An Automated White Blood Cell Nucleus Localization and Segmentation using Image Arithmetic and Automatic Threshold”, Journal of Applied Sciences ,2010.
[15] Subrajeet Mohapatra , Department of Electrical Engineering National Institute of Technology
Rourkela Rourkela- 769008, Orissa, “Automated Cell Nucleus Segmentation and Acute Leukemia
Detection in Blood Microscopic Images”, International Conference on Systems in Medicine and Biology 16-18 December 2010.
[16] Yang Song, Department of Computer Science and Engineering, the Pennsylvania State University, USA, “IKNN: Informative K-Nearest Neighbor Pattern Classification”, Springer-Verlag Berlin Heidelberg 2007.
[17] Digital Image Processing by Gonzalez Woods and Eddins.
[18] http://www.dti.unimi.it/fscotti/all
[19] Rohit Pathology, Dr. P.N.Patil, Jalgaon, Maharashtra, India.
دیدگاه ها