
نارسايي مهره کمر و سرطان ستون فقرات دو بيماري رايج است که سلامت بسياري را به خطر انداخته است. پس از بيماري هاي قلبي-عروقي، دومين عامل مرگومير در کشورهاي پيشرفته و سومين عامل مرگ ومير در کشورهاي کمتر توسعه يافته، سرطان است. درد کمر از 9/3 در سال 1992 به 3/14 درصد در سال 2018 افزايش يافته است. تحقيق در زمينه ايمپلنت هاي استخواني و تأثير آنها بر رفتار سلول هاي سرطاني ميتواند به کاهش مشکل کمک کند. از آن جا که مهره هاي کمر وظايف خاصي از جمله حفظ تعادل بدن و بافته اي نرم سامانه عصبي و ارگان هاي اطراف شکم و لگن دارند، آسيب به اين مهره ها ميتواند کيفيت زندگي را دچار اختلال کند. در بعضي موارد دارودرماني و تمرينات ورزشي در بهبود سلامت فرد اثرگذار نيستند و جراحي ضرورت مييابد. ابزارهاي ارتوپدي فلزي در دهه هاي اخير کاربردهاي وسيعي در اصلاح نافرمي مهره هاي ستون فقرات يافته اند و همواره گزينه مناسبي براي بهبود شرايط بوده اند اما توسعه مواد زيستسازگار کاراتر بوده و از اهميت بيشتري برخوردار است.
فلزات به سبب استحکام زياد، مورد توجه هستند. لکن به سبب مدول يانگ بالاتر از استخوان، باعث ايجاد سپرتنشي و در نتيجه شل شدن ايمپلنت ميشوند. درحاليکه مدول يانگ استخوان طبيعي GPa 20-5/ است، مدول يانگ آلياژ کبالت کروم موليبدن GPa 240، فولاد زنگ نزن GPa 200 و نايتينول GPa 50-30 است. که بايد به نحوي کاهش يابد. ايجاد تخلخل در ايمپلنت هاي فلزي ميتواند باعث کاهش مدول يانگ و نزديکترشدن مدول آنها به استخوان شود. ايجاد تخلخل باعث تسريع روند رشد استخوان نيز ميشود. نايتينول آلياژي است با ترکيبي از نرمي و سفتي و خواص منحصر به فردي همچون حافظه داري و سوپرالاستيسيته. از جمله خواص اين آلياژ ميتوان به زيست سازگاري، خصوصيات مکانيکي مطلوب، مقاومت به سايش و خوردگي خوب، خستگي و فرسايش مناسب، قابليت کاربرد بايو داشتن و مدول الاستيک پايين آن که نزديک به استخوان طبيعي است، اشاره کرد. اما در نوع پرنيکل آلياژ، زيستسازگاري تحت تأثير قرار گرفته و ممکن است پاسخ هاي آلرژيک مشاهده شود. تحقيقات نشان داده اند که يون هاي نيکل در طول درمان ميتوانند از آلياژ رها شوند.
اصلاح سطح يکي از راه کارهايي است که ميتواند از ميزان رهايش نيکل از سطح آلياژ Ni-Ti بکاهد و موجب افزايش زيست فعالي و يکپارچگي با بافت استخوان شود. زيستفعالي در آلياژهاي نايتينول ميتواند به روش هاي مختلفي همچون عمليات گرمايي، پاشش پلاسمايي، تابش پرتو يوني، تکنيک سل-ژل، اصلاح سطح شيميايي با محلول اسيدي يا قليايي مانند هيدروکسيد سديوم و عمليات اکسيداسيون با محلول پراکسيد هيدروژن افزايش يابد. عمليات قليايي سبب تشکيل لايه تيتانات سديم بر سطح نمونه ميشود. درحاليکه عمليات با پراکسيد هيدروژن تشکيل لايه ژلي از تيتانيا روي سطح ميدهد. تيتانات سديم و ژل تيتانيا توانايي ايجاد رسوب آپاتيت شبه استخواني در محيط آزمايشگاهي و کلينيکي داشته و از اين منظر، زيست فعال تلقي مي شوند. غوطه ور کردن نمونه هاي آلياژي NiTi در محلول اسـيدي حاوي H2 O2 و 3 HNO و در محلـول قليـايي حاوي NaOH از جمله روش هاي اصلاح سـطح اسـت کـه بـراي زيـست فعـال کردن آليـاژ بعـد از قرارگيـري در محلـول SBF اسـتفاده ميشود.
در يک تحقيق علمي، نمونه نايتينول تحت اصلاح حرارتي و سپس قليايي در محلول NaOH با غلظت هاي مختلف در دماي 110 درجه سانتيگراد به مدت 2 ساعت قرار گرفت. افزايش زيستفعالي بر اثر اصلاح قليايي نتيجه شد. نتيجه يک مطالعه ديگر که از روش هيدروترمال و عمليات قليايي-حرارتي براي افزايش زيست فعالي آلياژ نايتينول، استفاده کرده بود نيز مبين وجود لايه اي از اکسيد تيتانيوم در سطح و افزايش زيستفعالي بوده است. لازم به ذکر است که عمليات قليايي در زيستفعال کردن سطح فلز تانتاليم نيز مؤثر واقع شده است. همچنين پيشنهاد شده است که اصلاح سطح تيتانيم با اچ اسيدي ميتواند تأثيري مثبت بر يکپارچگي کاشتني هاي استخواني داشته باشد. محققان در يک مطالعه به اين نتيجه رسيدند که اصلاح سطح با محلول هاي اسيدي ميتواند مورفولوژي سطح را تغيير دهد و باعث افزايش زبري شود که اين پديده خود ميتواند باعث افزايش پيوند استخواني در ايمپلنت و کاهش اثر سمي نيکل به واسطه تشکيل يک لايه همگن و پايدار از اکسيدهاي تيتانيم در بدن شود و ميزان چسبندگي سلولي، رشد و تکثير گروه اصلاح شده و تغيير قابل ملاحظه اي نسبت به سطح اصلاح نشده نشان داد. در مطالعه اي ديگر براي ايجاد خاصيت زيست فعالي در سطح از اسيدکلريدريک و پراکسيد هيدروژن استفاده شد. با اين توضيحات، مشخص ميشود که تحقيق براي اصلاح سطح و ارتقا زيست فعالي آلياژ نايتينول تاکنون سير تکاملي داشته است. هدف اين پژوهش، ارتقاء باز هم بيشتر زيست فعالي از طريق بررسي اثر محلول هاي اسيدي قوي و به دنبال آن عمليات قليايي-حرارتي بر سطح با تعيين تأثير تغييرات سطحي بر افزايش قابليت زيست فعالي آلياژ است.
روش تحقيق
آلياژ نايتينول استفاده شده در اين تحقيق به روش ذوب القايي شمش نيکل کاتدي با خلوص 9/99 درصد وزني و تيتانيوم اسفنجي با خلوص 5/99 درصد وزني تهيه شد. جزئيات روش ساخت در مقاله ديگري ذکر شده است. با نورد داغ شمش توليدي، ورق NiTi به ضخامت يک ميليمتر مطابق روش ذکر شده در رفرانس توليد شد و سپس تحت برش دقيق توسط دستگاه وايرکاتر به نمونه هاي قرصي شکل داراي قطر دو ميليمتر بريده شد. سپس سطح نمونه ها با استفاده از سنباده مورد عمليات صيقلکاري مکانيکي قرار گرفته و با استن شسته شد. عمليات اصلاح سطح با استفاده از محلول حاوي HF-HNO3-H2O2 در شرايطي مشابه با روش ذکر شده در رفرانس انجام شد. نمونه شماره 1 در 9 ميلي ليتر محلول HF-HNO3-H2O2 با نسبت هاي 1:3:5 به مدت 8 دقيقه غوطه ور شد. سپس نمونه از محلول خارج شده و بلافاصله به منظور از بين رفتن آلودگي هاي سطحي در 4 بازه زماني 30 دقيقه اي به طور مجزا به ترتيب در ml ۲۰ استون، پروپانول، الکل و آب دي يونيزه در محفظه اولتراسونيک شستشو داده شد و با استفاده از خشک کن الکتريکي سطح نمونه در هواي معمولي خشک شد. نمونه تميز و خشک آنگاه درون ظرف تفلون حاوي محلول 5 مولار NaOH قرار گرفته و ظرف را داخل محفظه اتوکلاو به مدت 4 ساعت در آون با دماي 120درجه گرم نگه داشته شد. سپس ظرف حاوي نمونه را از اتوکلاو خارج کرده و براي خشک شدن، 24 ساعت در دماي محيط قرار داديم. نمونه شماره 2، که به عنوان شاهد در نظر گرفته شد، تحت عمليات سنباده زني و شستشوي اولتراسونيک، مشابه نمونه 1، قرار گرفت.
بررسي مورفولوژي سطح نمونه ها با ميکروسکوپ الکتروني گسيل ميداني مدل (MIRA3TESCAN-XMU (FESEM انجام شد. سلولهاي سرطاني MDA-MB231، با استفاده از محيط کشت (DMEM, GIBCO, England) و افزودن ۱۰% سرم جنين گوساله (FBS, GIBCO, England) و 1% پني سيلين – استرپتومايسين (GIBCO, England) کشت داده شدند تا سلول براي چسبندگي و رشد و تکثير آماده شود. علت استفاده از سلول سرطاني، در اختيار بودن سلول به علاوه سعي بر ايجاد شرايط رشد سريعتر به منظور افزايش دقت تشخيص بود. شکل 1 نشانگر سلولها در فلاسک کشت است که با ميکروسکوپ معکوس و بزرگنمايي X200 گرفته شده است.
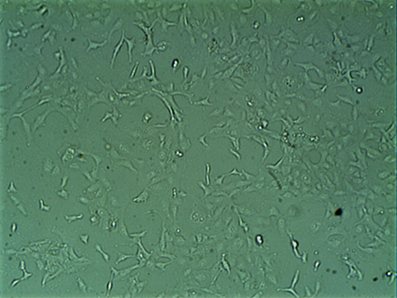
شکل ۱) تصویر سلولهایMDA-MB231 در فلاسک کشت
به منظور بررسي تأثير بيولوژيکي نمونه هاي نايتينول بر سلولهاي MDA-MB231، نمونه ها با رعايت شماره در دو خانه پليت قرار داده شدند و سپس 4 ميلي ليتر محيط کشت کامل به همراه مقدار مشخصي سلول در هر خانه ريخته شد به اين صورت که روي سطح نمونه ها را به طور کامل پر کند. سپس پليت در انکوباتور قرار گرفت، بعد از 4 ساعت پليت را زير ميکروسکوپ معکوس قرار داده و از چسبندگي سلول اي MDA-MB231 اطمينان حاصل شد. سپس پليت را مجدداً به انکوباتور بازگردانده و 24 ساعت در آنجا قرار داديم. روز بعد نمونه ها را به يک پليت عاري از محيط کشت و سلول منتقل کرده و از فرمالدهيد 07/0 درصد به منظور فيکس کردن سلول ها و آماده سازي براي تصويربرداري استفاده شد. به منظور مشاهده بهتر سلول ها توسط ميکروسکوپ الکتروني گسيل ميداني مدل VEGA\\TESCAN-LMU، ورقه نازک طلا را به عنوان پوشش رسانا روي سطح نمونه ها قرار داده وتصويربرداري انجام شد.
نتايج و بحث
شکل 2 سطح نمونه شاهد پس از صيقل کاري را نشان ميدهد. روي شکل تنها تصوير خطوط سنباده ديده ميشود؛ درحاليکه شکل 3 تصوير فرورفتگي هاي حاصل از تأثير محلول 1:3:5 HF-HNO3-H2O2ا FESEM را در معرض ديد قرار ميدهد. به نظر ميرسد اصلاح سطح، باعث ايجاد زبري و تخلخل سطحي بر نمونه نايتينول شده است. براساس تحقيقات قبلي، عمليات سطحي با محلول هاي حاوي اسيد فلوئوريدريک ميتواند سبب ايجاد حفرات نانو در سطح شود. هيدروژن پراکسيد به دليل دارا بودن اکسيژن فعال با سطح تيتانيوم واکنش داده و باعث به وجود آمدن ژل اکسيد تيتانيوم روي سطح آلياژ شده و به عنوان يک مانع شيميايي در برابر رهايش يون نيکل در کاشتني عمل خواهد کرد. اما اسيد نيتريک با نيکل آلياژ واکنش داده و ضمن ايجاد خلل و فرج هاي ريز سطحي، لايه اي حاوي اکسيد تيتانيوم بر سطح آلياژ باقي ميگذارد.
(1)
3NiTi(s)+12 HNO3(aq) =3Ni(NO3)2(aq)+ 3TiO2(s)+6NO(g)+6H2O(aq)q
در ادامه نشان داده خواهد شده که اين تغييرات باعث افزايش چسبندگي، زيست فعالي و تسريع روند رشد استخوان خواهند شد.

شکل۲) تصویر FESEM میکروسکوپ الکترونی سطح نمونه شاهد (شماره ۲)

شکل 3) تصویر FESEM سطح نمونه NiTi غوطه ور شده در محلول HF-HNO3-H2O2 به مدت ۸ دقیقه (شماره ۱)
مطابق با يافته هاي محققين قبلي، زماني که نمونه غوطه ور در محلول سود داخل بوته تفلاني درون اتوکلاو قرار داده شده و تحت عمليات هيدروترمال قرار ميگيرد، يک لايه اکسيدي مقاوم به خوردگي و سايش بر سطح نمونه تشکيل شده و سبب بهبود خواص سطحي و بيولوژيکي نمونه ميشود. اين لايه مخلوطي از دو ترکيب TiO و TiO2 است که زيست سازگاري بهتري نسبت به Ti دارد. وجود لايه سطحي TiO2 ميتواند مانع آزاد شدن بالقوه نيکل شود. شکل 4 تصوير سطح آلياژ نايتينول بدون عمليات اصلاح سطح (نمونه شاهد) را پس از کشت سلول نشان ميدهد. چسبندگي و رشد سلول قابل توجهي در اين تصوير ملاحظه نميشود. درحاليکه تصوير نمونه 1 پس از عمليات هيدروترمال و کشت سلولي (شکل 5)، بيانگر چسبندگي و زنده ماني قابل ملاحظه سلول ها است. هر سه پديده ايجاد لايه اکسيد، افزايش تخلخل سطحي و بيشترشدن زبري ميتوانند عامل افزايش چسبندگي و زنده ماني سلولي محسوب شوند.

شکل 4) تصویر سطح نمونه شماره ۲ پس از کشت سلول

شکل ۵) سطح نمونه شماره ۱ اصلاح سطح شده بعد از کشت سلول
به طورکلي در حدود چند دهه پيش، مطالعاتي براي گسترش سطوح تيتانيمي غيرپوششي آغاز شد. گزارش شده است که جذب فيبرونکتين روي سطوح خشن کمتر از سطوح صاف است. فيبرونکتين يک گليکوپروتئين است که به طور سريعي به سطوح سخت چسبيده و در نتيجه باعث چسبيدن سلول هاي ديگر ميشود. ميکروتوپوگرافي سطح ميتواند بر تعداد و مورفولوژي پاهاي کاذب چسبنده سلول و جهت گيري سلول ها تأثير گذاشته و مهاجرت سلول ها به داخل حفره هاي موجود در سطح ماده کاشتني را هدايت کرده و در نتيجه رشد استخوان را افزايش دهد. اين موضوع، با انرژي سطحي کاشتني و به عبارت ديگر ميزان آبدوستي سطح ارتباط دارد. از مطالب بالا ميتوان نتيجه گرفت که زبري و شيمي سطح نقش فوق العاده مهمي را در رفتار سلول بر روي سطح ايمپلنت ايفا ميکند.
نتيجه گيري
سطح آلياژ نايتينول ساخته شده به روش ذوب القايي-انجماد شمش-نورد داغ تحت تأثير محلول اسيدي متشکل از اسيدهاي سه تائي (HF-HNO3-H2O2) و فرآيند روش هيدروترمال تغييرات مثبت قابل توجهي را متحمل ميشود. اين تغييرات سبب ايجاد تخلخل، زبري و زيست فعالي سطحي شده و آلياژ را به عنوان گزينه اي مناسب براي ترميم ضايعات بافت سخت، آماده ميکند. براساس مطالعات کشت سلولي، استفاده از روش اصلاح سطح انتخابي، باعث بهبود چسبندگي، رشد و تکثير سلولي و اتصال بهتر و ايمنتر کاشتني ارتوپدي با بافت زنده اطراف خواهد شد.
منابع
[1] A. Kamanli, G. Karaca, A. Kaya, M. Koc, H. Yildirim. Conventional physical therapy with lumbar traction; clinical evaluation and magnetic resonance imaging for lumbar disc herniation, Bratisl Lek Listy; 111(10), 2010: 4-541.
[2] H. Yoshihara. Rods in spinal surgery: a review of the literature, The Spinal Journal, 13, 2013: 1350-1358.
[3] D. Kok, M. Grevitt, F.H. Wapstra , A.G. Veldhuizen. The Memory Metal Spinal System in a Posterior Lumbar Interbody Fusion (PLIF) Procedure: A Prospective, Non-Comparative Study to Evaluate the Safety and Performance, The Open Orthopedics Journal, 6, 2012: 220-225.
[4] S.A. Hosseini, S.K. Sadrnezhaad, A. Ekrami. Phase transformation behavior of porous NiTi alloy fabricated by powder metallurgical method, Materials Science and Engineering C, 29, 2009: 2203–2207.
[5] S. Parvizi, V. Hasannaeimi, E. Saebnoori, T. Shahrabi, S.K. Sadrnezhaad. Fabrication of Porous NiTi Alloy via Powder Metallurgy and Its Mechanical Characterization by Shear Punch Method, Russian Journal of Non-Ferrous Metals, 53(2), 2012: 169–175.
[6] S. Parvizi, H. R. Hafizpour, S. K. Sadrnezhaad, A. Akhondzadeh , M. Abbasi Gharacheh. Neural network prediction of mechanical properties of porous NiTi shape memory alloy, Powder Metallurgy, 54(3), 2011: 450-454.
دیدگاه ها